
近日,上海交通大学医学院附属仁济医院检验科李敏课题组在国际知名学术期刊《外泌体杂志》(journal of extracellular vesicles, if=25.841)上在线发表了人体共生菌囊泡与细菌竞争的最新研究成果,证实了囊泡在细菌分泌疏水性抗菌分子及活性发挥中的必要作用。
人类生存的环境里存在亿万个细菌、病毒,经过数亿年的进化,一些对人体有益的细菌与人体共存,成为了人类共生菌。而生物的生存目标都是一样的,即生存繁衍下去,通过自己进化出的竞争优势,保留“朋友”,消灭“敌人”。仁济医院的这一研究成果,即发现人体共生菌分泌的囊泡,对消灭有害细菌、病毒起到了关键性作用。
此前学界已达成共识:共生菌通过分泌抗菌分子来提高竞争活性,不过,人体是个“水环境”,疏水性抗菌分子(即不溶于水的抗菌分子)是怎样在人体中“游到”靶细菌(即要杀死的细菌)那儿的呢?
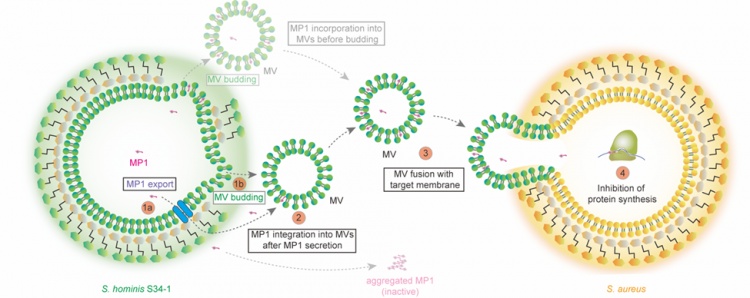
本研究的李敏课题组,此前已经发现并报道了人体共生菌分泌疏水性抗菌分子微球菌素(mp1),深入研究发现:有活性的mp1并不是以游离单体的形式存在,而是被囊泡包裹着运送到靶细菌,进而抑制靶细菌的蛋白合成。
据了解,细菌囊泡是脂质双分子层的球体结构,在细菌中,囊泡的产生是无处不在的。囊泡可以包裹核酸、毒素、酶、信号分子和耐药因子等,在细菌的毒力、耐药、信号传导和生物膜形成等中发挥重要的作用。
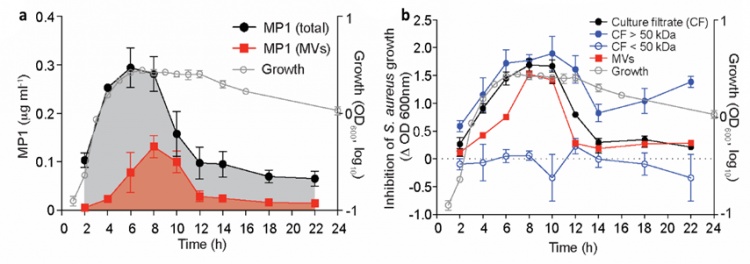
该团队发现人体共生菌囊泡的抗菌活性曲线和上清抗菌活性的曲线具有极高的匹配度。进一步,李敏团队验证了无论在体外还是体内,只有囊泡包裹的mp1才具有极好的抗菌活性。
研究者进一步提供了此前无法获得的证据,即囊泡是通过膜融合的方式将mp1呈递给靶细菌,进而抑制靶细菌的蛋白合成。
本研究证明了囊泡是细菌分泌的疏水性抗菌分子发挥活性的必要形式,不同于简单地提高疏水性分子的水溶性,囊泡包裹的策略可以对该分子实现高度的浓缩、长途运输以及与靶细菌的膜融合。囊泡在细菌生理学中提供了一种必不可少的功能,而不仅仅是附属功能。

该论文第一作者为上海交通大学医学院附属仁济医院检验科刘瑶博士,刘瑶博士也是2020年microbiome(if:14.65)文章的第一作者;通讯作者为上海交通大学医学院附属仁济医院检验科李敏教授和美国国立卫生研究院michael otto教授。
栏目主编 张琪
责任编辑 徐玲
图片来源 受访单位供图
上观号作者:浦东观察
